病员监护仪出口核查指南来了!谨防出口扣货、退货!下面跟着瀚而普出口外贸代理小编一起来看看吧!更多出口外贸代理欢迎来电咨询瀚而普上海外贸进出口公司,服务热线:021-35383360
今年4月10日,海关总署发布了2020年第53号公告,对医用口罩、医用防护服、病员监护仪等11类海关商品编号项下的医疗物资实施出口商品检验,加强医疗物资出口质量监管。
面对国外严峻的疫情,海外防疫物资需求持续增长,国内企业对医疗设备及医疗用品的出口关注度越来越高,下面发布君重点来介绍一下病员监护仪出口的关注点。
首先,让我们来认识一下病员监护仪
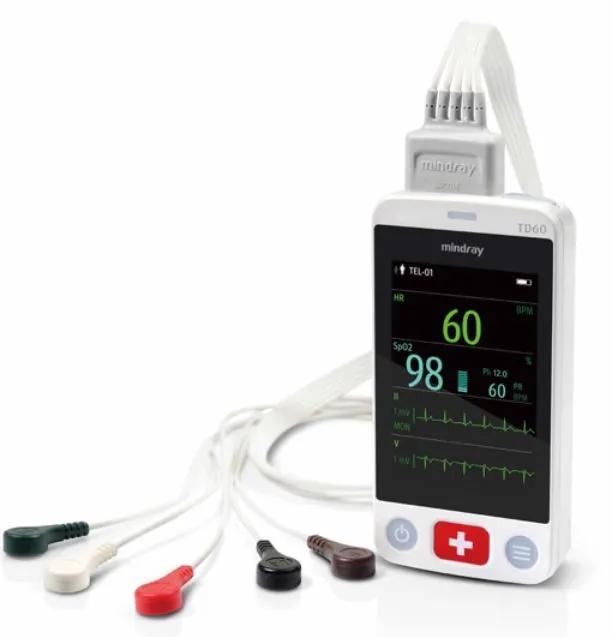
产品定义
病员监护仪通常由主机、供电电源、显示器、一个或多个生理参数功能模块和报警系统组成,从单一患者处采集参数信息,处理、显示信息并发出报警。
该类产品在我国《医疗器械分类目录》中属于07大类“医用诊察和监护器械”中一级产品类别“监护设备”、二级产品类别“病人监护设备”,用于对患者的一个或多个生理参数进行测量和监护,常见的生理参数有:心电、心率、脉搏率、呼吸、氧饱和度、血压、体温、脑电、肌电等,也包括对有创参数、麻醉气体浓度等进行监测。代表产品有病人监护仪、多参数监护仪等,也包括呼吸气体监护仪、麻醉气体监护仪等。
相似产品区分
与商品编码9018193010病员监护仪相近的产品有商品编码9018110000的心电图记录仪、9018902000的血压测量仪器及器具等。病员监护仪的特点是必须要对一或多个生理参数进行较长时间的监控,在参数异常时能报警。因此仅有记录功能的心电图记录仪、短时测量的血压计、血氧饱和度测量仪等商品不属于该类别。
对于多功能商品,必须要对商品的主要功能进行分析来确认产品是否属于该商品编码。
病员监护仪出口核查要点
商品编码为9018193010的病员监护仪都属于医用,需重点核查是否提交了医疗器械产品注册证明和质量安全承诺证明。
商品的标识和说明书是重点。标识、说明书信息必须保持一致。核查标识是否粘贴或固定牢固,内容应清晰易于辨识。标识上应有商品名称、型号、生产日期、注册人/生产企业名称和地址,注册证书编号,产品执行标准等信息。电源参数、警告标识和警告用语应靠近相应部位。
对于多部件组装的监护仪,每个生理监护单元应有制造商名称或商标、以具体名称或以参考数字、字母标识的型号,序列号信息。


通过政府注册管控信息进行查询
病员监护仪在各国都依据医疗器械管理要求实施注册或管控,可通过相关注册管控信息进行核查。
我国病员监护仪的主要出口国家和地区有美国、欧盟、俄罗斯、土耳其、非洲、印度等。
01中国
China
病员监护仪在中国属于二类或三类医疗器械,实行注册制,可以在国家药品监督管理局http://www.nmpa.gov.cn医疗器械查询栏目查询国产/进口医疗器械产品(注册)情况。
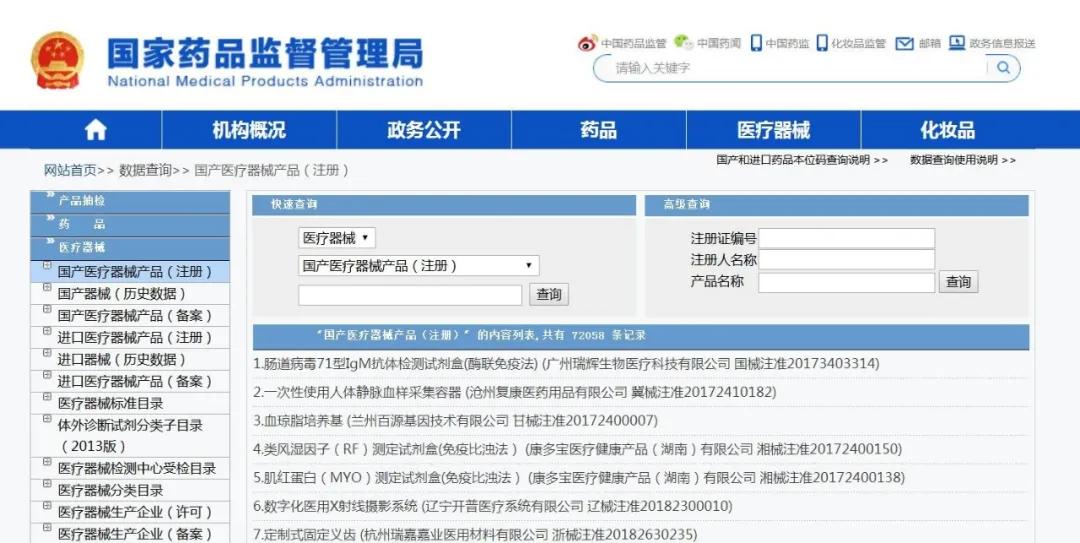
02美国出口
病员监护仪在美国属于II类医疗器械,由美国食品药品监督管理局(FDA)管理,须通过510K上市前通告,获得工厂注册和医疗器械列名后方可在美国上市。
美国主要的病员监护仪产品类别如下表
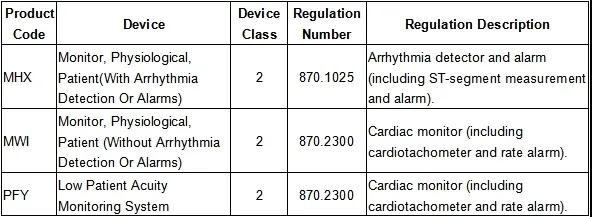
已获得美国FDA准入的产品可以通过其官网查询注册证书号进行查询,链接为:https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPMN/pmn.cfm
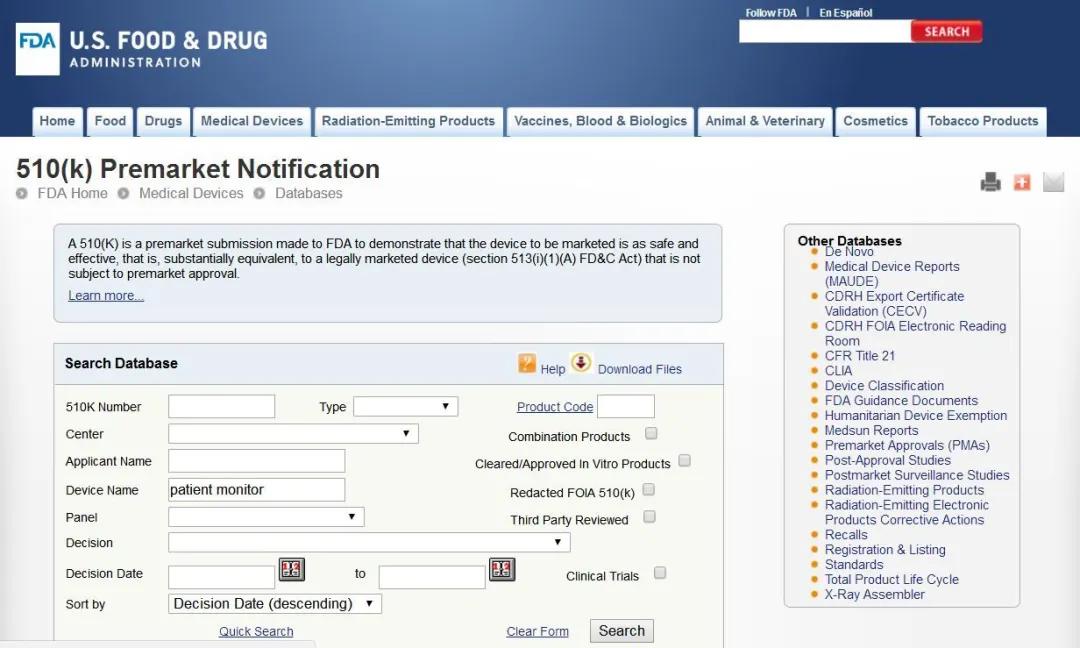
03欧盟出口
在欧盟销售的病员监护仪必须加贴CE标志。在上市前必须实施欧盟相关指令(93/42/EEC“MDD”)或法规(EU 2017/745“MDR”)规定的合格评定程序。欧盟为保证这些合格评定程序的有效性,从各成员国的第三方合格评定机构中统一认定了一批“公告机构”(Notified Body,NB)负责参与除I类医疗器械外的合格评定程序,授权其对产品和制造商的质量体系/产品设计检验实施上市前审查,为审查合格的产品颁发证书。产品获得证书后才可加贴CE标志。
欧盟网站,可查询每类产品的准入要求,符合性声明要求、协调标准等。
病员监护仪在欧盟属于IIa、IIb类医疗器械,每个合格的产品都必须有一个符合性声明Declaration of conformity,其中标注了产品信息,公告机构信息,符合的法规、标准等。

可通过获得授权的公告机构进行查询,欧盟医疗器械指令EU 93/42/EEC(MDD)授权的公告机构查询地址为:https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13。在Products 处选择MD 1300- Monitoring Devices或相关类别。
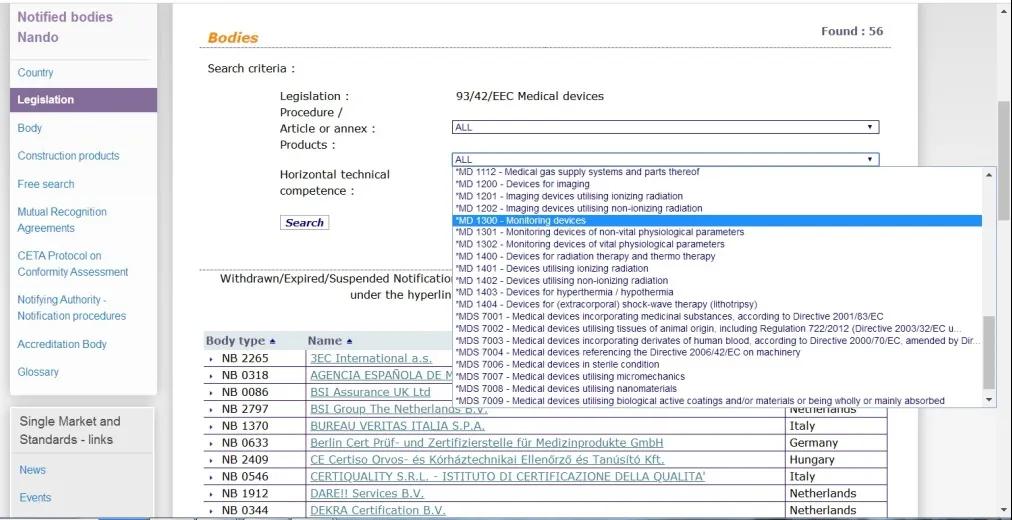
欧盟医疗器械条例EU 2017/745(MDR)授权的公告机构查询地址为:https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34。
通过上述链接,可进入发证机构官网,或者直接进入发证机构官网,可在线查询证书的相关信息。
04日本出口
病员监护仪在日本属于风险II或风险III类医疗器械。出口到日本的病员监护仪,必须满足日本“独立行政法人 医药品医疗器械综合机构” Pharmaceutical and Medical Device Act (PMD Act)的要求,PMDA要求国外的制造商必须注册制造商信息, PMDA网址为:https://www.pmda.go.jp/PmdaSearch/kikiSearch/。
05澳大利亚出口
病员监护仪出口澳大利亚须通过TGA注册,TGA的全称是治疗商品管理局Therapeutic Goods Administration。目前,澳大利亚与欧盟之间达成互认协议,已经获得CE认证的商品,向TGA提交申请后,可获得TGA证书。TGA网址:www.tga.gov.au,首页的Search databases栏目可获得注册产品的相关信息。
06俄罗斯出口
根据法规GOST R 51609-2000的要求,病员监护仪属于中等风险产品(Ⅱa)或者较高风险产品(Ⅱb)类医疗器械。俄罗斯要求医疗器械产品必须进行注册,同时产品还必须通过俄罗斯国家标准认证后才能上市销售和使用。
07土耳其出口
虽然土耳其未加入欧盟,但土耳其对医疗器械的认证管控要求参照欧盟CE要求,进入本国的医疗器械需提供CE符合性声明外,商品上也需加贴CE标志。
08南非出口
南非目前尚未有完善的医疗器械监管体制,仅由南非卫生署辐射控制部负责监管电磁(辐射)类医疗器械。但市场上有强烈地呼声,希望以FDA批准或CE认证作为产品上市的条件。
上海瀚而普国际贸易有限公司是一家以进口外贸代理、出口外贸代理及自营各类商品和技术的进出口业务、国际供应链业务为主的专业化、多功能、综合性的出口外贸代理公司,24小时应急响应,提供出口外贸代理、清关等一揽子进出口服务,出口外贸代理热线:021-35383360。
转自网络,如侵删。







 关注瀚而普微信号
关注瀚而普微信号